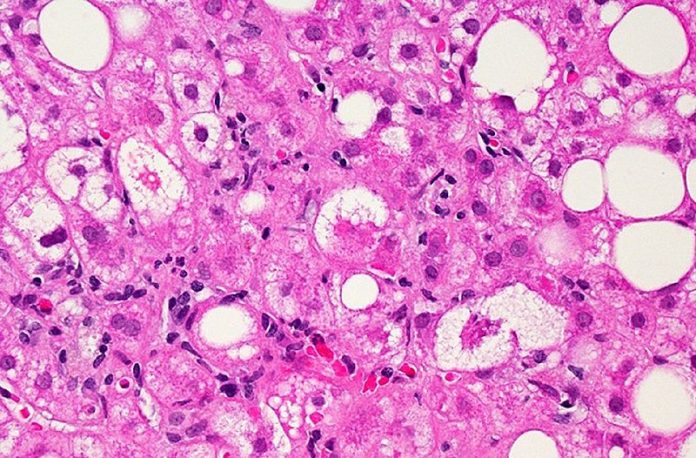
Rezdiffra (resmetirom) ได้รับการอนุมัติจาก FDA ของสหรัฐอเมริกา สำหรับการรักษาผู้ใหญ่ที่มีภาวะไขมันพอกตับอักเสบที่ไม่มีแอลกอฮอล์ (NASH) ที่ไม่เป็นโรคตับแข็ง โดยมีแผลเป็นในตับระดับปานกลางถึงรุนแรง (พังผืด) โดยใช้ร่วมกับการควบคุมอาหารและการออกกำลังกาย
จนถึงขณะนี้ ผู้ป่วยโรคไขมันพอกตับอักเสบที่ไม่มีแอลกอฮอล์ (NASH) ที่ไม่ใช่โรคตับแข็งและมีแผลเป็นที่ตับอย่างเห็นได้ชัด ยังไม่มียาที่สามารถช่วยรักษาผู้ป่วยได้โดยตรง ความเสียหายของตับ. อย approval of Rezdiffra will, for the first time, provide a การรักษา option for these patients, in addition to diet and exercise.
NASH is a result of the progression of non-alcoholic fatty ตับ โรค ที่ไหน ตับ inflammation, over time, can lead to liver scarring and liver dysfunction. NASH is often associated with other health problems such as high blood pressure and type 2 diabetes. By at least one estimate, approximately 6-8 million people in the U.S. have NASH with moderate to advanced liver scarring, with that number expected to increase.
Rezdiffra เป็นตัวกระตุ้นบางส่วนของตัวรับฮอร์โมนไทรอยด์ การกระตุ้นตัวรับนี้โดย Rezdiffra ในตับช่วยลดการสะสมไขมันในตับ
ความปลอดภัยและประสิทธิภาพของ Rezdiffra
The safety and efficacy of Rezdiffra was evaluated based on an analysis of a surrogate endpoint at month 12 in a 54-month, randomized, double-blind placebo-controlled trial. The surrogate endpoint measured the extent of ตับ inflammation and scarring. The sponsor is required to conduct a postapproval study to verify and describe Rezdiffra’s clinical benefit, which will be done through completing the same 54-month study, which is still ongoing. To enroll in the trial, patients needed to have a ตับ biopsy showing inflammation due to NASH with moderate or advanced ตับ scarring. In the trial, 888 subjects were randomly assigned to receive one of the following: placebo (294 subjects); 80 milligrams of Rezdiffra (298 subjects); or 100 milligrams of Rezdiffra (296 subjects); once daily, in addition to standard care for NASH, which includes counseling for healthy diet and exercise.
At 12 months, liver biopsies showed that a greater proportion of subjects who were treated with Rezdiffra achieved NASH resolution or an improvement in liver scarring as compared with those who received the placebo. A total of 26% to 27% of subjects who received 80 milligrams of Rezdiffra and 24% to 36% of subjects who received 100 milligrams of Rezdiffra experienced NASH resolution and no worsening of liver scarring, compared to 9% to 13% of those who received placebo and counseling on diet and exercise. The range of responses reflects different pathologists’ readings. In addition, a total of 23% of subjects who received 80 milligrams of Rezdiffra and 24% to 28% of subjects who received 100 milligrams of Rezdiffra experienced an improvement in ตับ scarring and no worsening of NASH, compared to 13% to 15% of those who received placebo, depending on each pathologist’s readings. Demonstration of these changes in a proportion of patients after just one year of treatment is notable, as the โรค typically progresses slowly with most patients taking years or even decades to show progression.
ผลข้างเคียงของการใช้ยาเรซดิฟรา
ผลข้างเคียงที่พบบ่อยที่สุดของ Rezdiffra ได้แก่ อาการท้องร่วงและคลื่นไส้ Rezdiffra มีคำเตือนและข้อควรระวังบางประการ เช่น ความเป็นพิษต่อตับที่เกิดจากยาและผลข้างเคียงที่เกี่ยวข้องกับถุงน้ำดี
Use of Rezdiffra should be avoided in patients with decompensated cirrhosis. Patients should stop using Rezdiffra if they develop signs or symptoms of worsening ตับ function while on Rezdiffra treatment.
ปฏิกิริยาระหว่างยาของ Rezdiffra
การใช้ยา Rezdiffra ร่วมกับยาอื่นๆ โดยเฉพาะยากลุ่มสแตตินในการลดคอเลสเตอรอล อาจส่งผลให้เกิดปฏิกิริยาระหว่างยาที่มีนัยสำคัญ ผู้ให้บริการด้านการดูแลสุขภาพควรดูข้อมูลการสั่งจ่ายยาฉบับเต็มเพื่อดูข้อมูลเพิ่มเติมเกี่ยวกับการโต้ตอบระหว่างยาที่มีนัยสำคัญกับ Rezdiffra ขนาดยาที่แนะนำ และการปรับเปลี่ยนการบริหาร
พื้นที่ องค์การอาหารและยา approved Rezdiffra under the accelerated approval pathway, which allows for earlier approval of drugs that treat serious conditions and address an unmet medical need, based on a surrogate or intermediate clinical endpoint that is reasonably likely to predict clinical benefit. The required aforementioned 54-month study, which is ongoing, will assess clinical benefit after 54 months of Rezdiffra treatment.
เรซดิฟฟราได้รับการรับรองการบำบัดแบบก้าวกระโดด การติดตามอย่างรวดเร็ว และการตรวจสอบลำดับความสำคัญสำหรับข้อบ่งชี้นี้
พื้นที่ องค์การอาหารและยา granted the approval of Rezdiffra to Madrigal Pharmaceuticals.
***
ที่มา:
FDA 2024 ข่าวประชาสัมพันธ์ – FDA อนุมัติการรักษาครั้งแรกสำหรับผู้ป่วยที่มีแผลเป็นในตับเนื่องจากโรคไขมันพอกตับ โพสต์เมื่อ 14 มีนาคม 2024 มีจำหน่ายที่ https://www.fda.gov/news-events/press-announcements/fda-approves-first-treatment-patients-liver-scarring-due-fatty-liver-disease
***